O gene FLT3 e sua importância na leucemia mielóide aguda (LMA)
Leucemia mielóide aguda (LMA) é um termo que alberga um grupo heterogêneo de doenças malignas, caracterizadas pela proliferação descontrolada de células precursoras hematopoéticas clonais.
Leucemia mielóide aguda (LMA) é um termo que alberga um grupo heterogêneo de doenças malignas, caracterizadas pela proliferação descontrolada de células precursoras hematopoéticas clonais. A proliferação celular autônoma se dá, dentre outras razões, pela ativação de receptores com atividade tirosinoquinase, os quais promovem uma cascata de fosforilação em proteínas intracelulares que culmina na progressão do ciclo celular. Ainda que a proliferação de células normais seja finamente regulada pela presença de fatores de crescimento e por sinais de adesão, nas células leucêmicas ocorre perda desse controle e a proliferação pode ser desencadeada de modo autônomo, frequentemente como conseqüência de mutações que causam a ativação constitutiva de receptores tirosinoquinase (Licht & Sternberg, 2005).
O FLT3 (FMS -fator estimulador de colônia de macrófagos- like tyrosine kinase) é um receptor com atividade tirosinoquinase expresso em célula precursora hematopoética e que desaparece conforme essas células se diferenciam. Tem importante papel na sobrevida, proliferação e diferenciação celular (Abu-Duhier et al, 2001, Small, 2006).
Observa-se expressão aumentada de FLT3 na LMA e mutações nesse gene compreendem uma das alterações somáticas mais comuns dessa doença, ocorrendo em cerca de 20 a 30% dos casos (Mrózek & Bloomfield, 2006; Krum, 2006). A mutação mais freqüente é a duplicação interna em tandem (DIT/FLT3) que consiste na duplicação de um segmento de 3 a 400 pares de base na região justa-membrana. A DIT/FLT3 leva à ativação constitutiva da tirosinoquinase, promovendo a autofosforilação do receptor e a fosforilação de várias outras proteínas, o que resulta em significativa alteração no padrão de expressão gênica das células comprometidas e inequívoco estímulo à proliferação (Pinheiro et al, 2007).
Embora os principais fatores prognósticos na LMA continuem sendo a idade do paciente e as alterações citogenéticas das células leucêmicas, diversos estudos demonstram que a presença de DIT/FLT3 oferece informações importantes nesse contexto por conferir prognóstico desfavorável (Small, 2006). A DIT/FLT3 tem sido observada com maior freqüência no subgrupo de pacientes com cariótipo normal, que são tradicionalmente estratificados como portadores de prognóstico intermediário. Nesse subgrupo, a DIT/FLT3 abre a perspectiva de discriminar pacientes com prognóstico desfavorável que serão beneficiados pela intensificação do tratamento. Nessa mesma linha, a presença de DIT/FLT3 em pacientes com alterações cromossômicas consideradas favoráveis, a exemplo da leucemia promielocítica aguda com t(15;17), pode permitir a identificação de casos com pior prognóstico e que mereçam cuidados adicionais na condução clínica (Chauffaille et al, 1996; Krum, 2006). Admite-se atualmente que a presença de DIt/FLT3 nos casos com alterações citogenéticas favoráveis, resulta em piora do prognóstico, por terem sido observadas, nesses pacientes, maior de taxa de morte na apresentação, menor sobrevida livre de eventos e associação com maior massa leucêmica e morte precoce (Yoo et al, 2006).
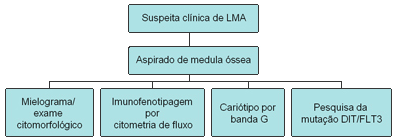
Em que pese a importância do cariótipo convencional como o pilar a partir do qual serão obtidas as principais informações prognosticas na LMA, estudos recentes têm revelado novos métodos moleculares que auxiliam na estratificação prognostica e na escolha da melhor opção terapêutica. Por sua importância na patogenia molecular e na estratificação prognóstica da LMA, a pesquisa de DIT/FLT3 tornou-se recentemente disponível em nosso meio e deverá ser incorporada à abordagem diagnóstica multifacetada de um paciente com LMA, juntamente com o mielograma, a imunofenotipagem e o cariótipo de medula óssea (figura 1).
Referências:
Abu-Duhier FM, Goodeve AC, Wilson GA, Care RS, Peake IR, Reilly JT. Genomic structure of human FLT3: implications for mutational analysis. Br J Haematol. 113(4):1076-7, 2001.
Chauffaille MLLF, Yamamoto M, Moncau JE, Braga GW, Souto EX, Kerbauy J. Cytogenetic abnormalities as prognostic factors in acute myeloid leukemia. Rev Assoc Med Bras 42(4):200-4, 1996.
Krum EA. Correlação entre cariótipo, duplicação interna em tandem do gene FLT3 e polimorfismo do códon 72 do P53 em leucemia mielóide aguda [tese]. São Paulo: Universidade Federal de São Paulo; 2006.
Licht JD & Sternberg DW. The molecular pathology of AML. Hematology ASH Education Book, 137-142, 2005.
Pinheiro RF, Moreira ED, Silva MR, Greggio B, Alberto FL, Chauffaille MLLF. FLT3 mutation and AML/ETO in a case of Myelodysplastic syndrome in transformation corroborates the two hit model of leukemogenesis. Leuk Res. 31(7):1015-8, 2007.
Small D. FLT3 mutations: biology and treatment. Hematology (Am Soc Hematol Educ Program) 178-184, 2006.
Yoo SJ, Park CJ, Seo EJ, Lee KH, Chi, HS. Inferior prognostic outcome in acute promyelocytic leukemia with alterations of FLT3 gene. Leuk Lymphoma 47: 1788-93, 2006.
Outros artigos
Ginecologista, o relógio biológico de sua paciente está correndo. Seu atendimento acompanha esse tempo?
Ginecologista, o relógio biológico de sua paciente está correndo.
Investigação de hiperprolactinemia e macroprolactina
Saiba como contornar os desafios na interpretação dos resultados da dosagem de prolactina
Strain atrial: uma nova ferramenta clínica para avaliação da função cardíaca
Strain atrial: uma nova ferramenta clínica para avaliação da função cardíaca
Nirsevimabe ajuda a prevenir a infecção e complicações causadas pelo VSR em lactentes
Nirsevimabe ajuda a prevenir a infecção e complicações causadas pelo VSR em lactentes